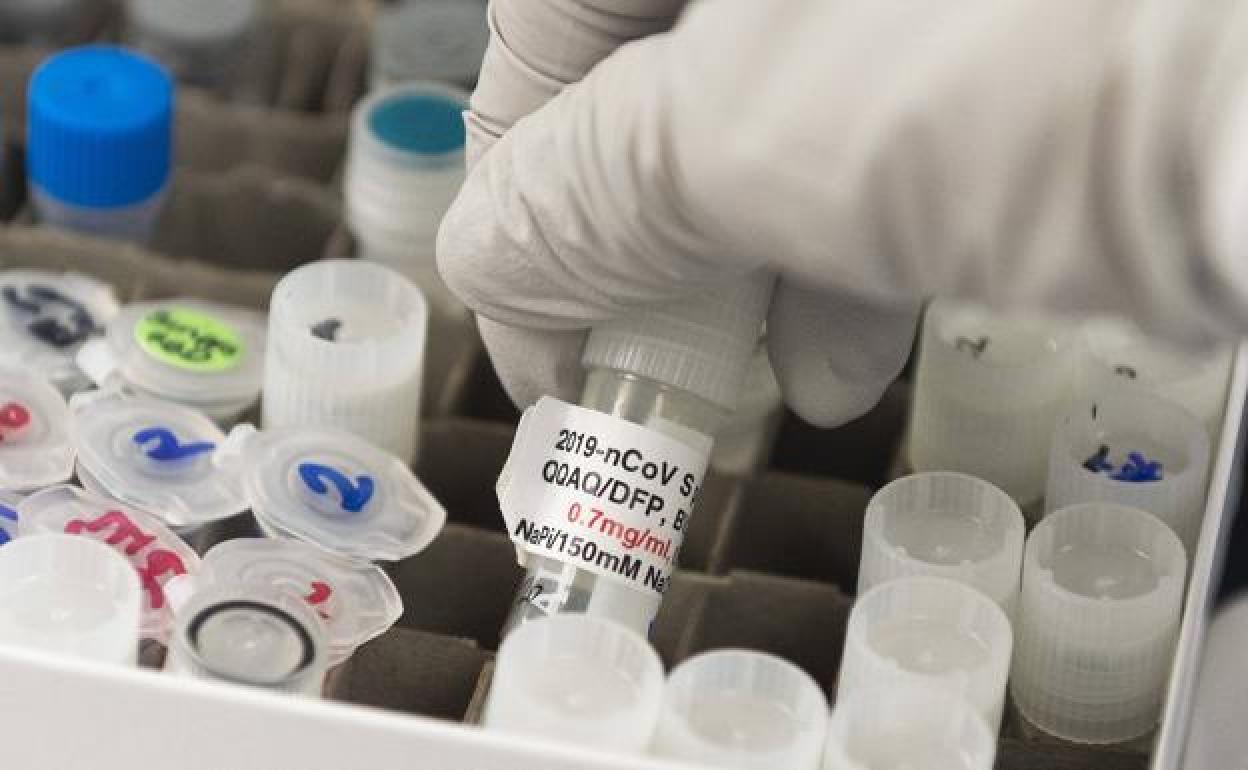
Coronavirus | Pfizer quiere involucrar a su planta española en la fase final de la vacuna
El eje de la compañía en Europa será su sede al norte de Bruselas, aunque habrá más centros embarcados en la distribución de la vacuna
MELCHOR SÁIZ-PARDO
MADRID.
Martes, 10 de noviembre 2020, 03:08
Es muy probable que España ponga su granito de arena en el esfuerzo mundial para sacar adelante una vacuna efectiva contra la covid, aunque no haya estado en el centro de las investigaciones ni en el desarrollo del proyecto. Los responsables de Pfizer estudian movilizar a buena parte de la planta biotecnológica de la localidad madrileña de San Sebastián de los Reyes para la parte del final de la producción de la sustancia y su distribución.
Portavoces de Pfizer no quisieron aclarar cuál será el papel de la planta madrileña, aunque diversas fuentes consultadas por este periódico explicaron que desde hace meses las instalaciones españolas se han ido transformado para apoyar en la fase final de la vacuna contra el coronavirus. Sergio Rodríguez, presidente y director general de Pfizer en España, afirmó este fin de semana en una entrevista en el 'El Global' que su compañía espera fabricar hasta 100 millones de dosis para finales de 2020 y aproximadamente 1.300 millones de dosis para fines de 2021. Pfizer -explicaron portavoces de la empresa en Madrid- tiene en proyecto que sus instalaciones de Puurs, al norte de Bruselas (Bélgica), sean el eje de su «suministro europeo», en el que su socio en este proyecto, la alemana BioNTech, «también formará parte de la red comercial».
Es en la planta de Saint Louis, Missouri, donde se fabrica el ADN plasmático del antígeno de la vacuna. Este ADN modelo se fabrica en un proceso de cultivo celular y, posteriormente, se purifica mediante una serie de pasos cromatográficos y de filtración. La segunda planta involucrada es la de Andover (Massachusetts), que se dedica a la fabricación de la «sustancia activa». A continuación, la sustancia activa se envía a Kalamazoom (Míchigan) para la «formulación, llenado y acabado» del producto.
Rodríguez, que anunció en otra entrevista en el 'El Economista' que su compañía solicitará la autorización para la fabricación de la vacuna a partir de la tercera semana de noviembre, recordó que en septiembre la multinacional cerró un preacuerdo con la Comisión Europea para un suministro propuesto de 200 millones de dosis a los estados miembros, con opción de suministrar 100 millones de dosis adicionales. Las entregas comenzarían a finales de 2020.
EEUU asegura que la vacuna tiene eficacia del 90%
El mundo recibió ayer una de las mejores noticias que cabría esperar en la lucha contra el coronavirus, aunque habrá que aguardar todavía, al menos, varias semanas más para que la esperanza se convierta en auténtica certeza. La compañía farmacéutica estadounidense Pfizer anunció que su vacuna contra la covid 19 logra una eficacia del 90%, un porcentaje que se sitúa muy por encima de lo requerido por los reguladores estadounidenses. El anuncio, realizado de manera simultánea en Estados Unidos y Europa -dada la asociación de Pfizer con la alemana Biontech-, disparó la Bolsa de Nueva York, a pesar de que en la investigación quedan aún datos por confirmar.
La carrera por la consecución de la primera vacuna que despierte el interés del mercado financiero occidental llega ahora a su momento más álgido. En ese contexto debe entenderse la información difundida ayer por Pfizer y Biontech, que según expertos consultados por este periódico es buena, pero con matices. Los prototipos desarrollados por Rusia y China que, conforme han anunciado sus respectivos Gobiernos, serían los más avanzados, aunque no han logrado despertar el interés de Europa y América del Norte. Mientras, el mundo occidental aguarda la llegada del primer prototipo propio que, desde que arrancó la crisis sanitaria, se está diciendo que llegaría para el cambio de año. Las fechas estarían así al caer.
La multinacional americana señaló, mediante una fría nota de prensa, estar en condiciones de asegurar que su prototipo protege frente al 90% de las infecciones provocadas por el nuevo coronavirus de Wuhan. «Hoy es un gran día para la ciencia y para la humanidad», afirmó el consejero delegado de Pfizer, Alberto Bourla, con un lenguaje épico. «Los primeros resultados de nuestra fase 3 (la que se lleva a cabo con humanos) de la vacuna de covid-19 otorgan evidencia inicial de la habilidad de nuestro prototipo para prevenir la infección. Tan alto nivel de eficacia se ha logrado tan solo siete días después de que los voluntarios recibieran la segunda dosis del preparado, es decir, 28 días desde que comenzaron las pruebas con este medicamento, que requiere dos pinchazos.
Las lagunas
Uno de los argumentos que sustenta la esperanza despertada por el proyecto es que se trata de un ensayo clínico a gran escala, con la participación de 44.000 personas. La muestra de la que Pfizer extrae sus resultados se limita, sin embargo, a 94 voluntarios que dieron positivo en las pruebas de detección de la infección. Unos recibieron la vacuna y otros, placebo, es decir un suero.
El trabajo es, de momento, incompleto. La compañía debería ampliar su estudio con los datos obtenidos de los análisis de, como mínimo, 164 infectados, que se supone que dispondrán en las próximas semanas. El informe final, además, debe ser comprobado aún por lo que en ciencia se llaman pares, otros equipos investigadores que siguiendo su misma metodología lleguen a los mismos resultados.
Aún así, la compañía asegura estar en disposición de contar con «dos meses de datos de seguridad acumulados» en la tercera semana de este mes de noviembre, lo que le permitiría satisfacer los requisitos de la Agencia de Alimentos y Medicamentos de Estados Unidos (la FDA) para pedir la autorización de emergencia. «Basados en nuestras proyecciones, esperamos producir globalmente hasta 50 millones de dosis en 2020 y luego hasta 1.300 millones en 2021», afirma la compañía.
El investigador Luis Enjuanes, director del laboratorio de coronavirus del Centro Nacional de Biotecnología del CSIC (Centro Superior de Investigaciones Científicas), considera «una buena noticia» la dada ayer por el laboratorio americano, «una empresa de confianza, con experiencia en vacunas y que -enumeró a favor del proyecto- desarrolla un trabajo con más de 40.000 voluntarios avalado por la FDA».
A la espera de que se conozcan nuevos datos sobre la investigación, añadió que tiene en su contra dos aspectos. El primero, que se trata de un medicamento que para su estabilización -para no echarse a perder- requiere ser mantenido a menos 70 grados centígrados bajo cero, lo que dificultará su administración, especialmente en los países más pobres, sin la infraestructura necesaria para algo así. Equipos de ese tipo en el mundo occidental solo existen en los hospitales, ni siquiera en los centros de salud.
Por otra parte, el medicamento de Pfizer necesita la aplicación de dos dosis para conseguir el efecto deseado. Enjuanes lo consideró, con todo, como «muy prometedor. Recordemos que Donald Trump les presionó para que tuvieran resultados antes de las elecciones; y éste y otros laboratorios contestaron que los tiempos de la ciencia no son los de la política», valoró el científico.
El comienzo del fin
Con todo, la investigadora Isabel Sola, que trabaja codo con codo con Enjuanes en un proyecto de vacuna similar al desarrollado por Pfizer y Biontech, se muestra más cauta en su valoración. El anuncio, según destaca en su análisis, se ha realizado antes de que se conozca el conjunto de los resultados y sin que se haya completado el pertinente estudio de seguridad, que hubiera requerido que pasaran al menos dos o tres semanas (no una) desde la aplicación de la segunda dosis para conocer el alcance de posibles efectos adversos. «Hay muchas incógnitas aún. No sabemos qué tipo de protección da: si impide la infección o permite superarla. Tampoco el grupo de edad al que se dirige, ni siquiera el tiempo que dura la inmunidad, Nos faltan datos», valora.
Enjuanes y Sola trabajan en uno de los proyectos de vacuna españoles más esperanzadores. Buscan un prototipo similar al de Pfizer y Biontech, pero que provoque una mayor respuesta inmunitaria con el fin de que baste un solo pinchazo para lograr la protección. Confían en lograrlo para finales de 2021. «Habrá sitio para todos en el mercado, porque se necesitarán muchas vacunas», confían. Entretanto, otras firmas internacionales, como Moderna y Astra Zeneca, intentan abrirse paso con sus propios prototipos también en los próximos meses. «Estamos en el comienzo del final», resume Sola. «Es esperanzador, pero nos queda camino».